Российские ученые на пути к спасению мозга от Альцгеймера и Паркинсона
И сследователи из Сеченовского университета совершили значимое открытие, выяснив, что белок теплового шока HSP70 способен эффективно защищать нервные клетки от разрушения, характерного для нейродегенеративных заболеваний. Ряд серьезных научных публикаций в ведущих международных журналах, включая Frontiers in Molecular Neuroscience, Applied Sciences и Laser Physics Letters, подтвердил мощный нейропротективный эффект HSP70. Этот эффект был зафиксирован в контексте таких тяжелых патологий, как боковой амиотрофический склероз (БАС), болезнь Паркинсона и болезнь Альцгеймера. Данные результаты открывают новые горизонты для разработки инновационных лекарственных препаратов, целью которых станет защита мозговых структур на молекулярном уровне.
Нейродегенеративные расстройства представляют собой обширную группу патологий, при которых происходит постепенная и необратимая утрата функций, а затем и гибель нервных клеток мозга. От этих заболеваний, которые могут быть как наследственными, так и связанными с возрастом, страдают миллионы людей по всему миру. До настоящего времени эффективные методы, способные остановить или обратить вспять процессы нейродегенерации, остаются недостижимыми.
В ходе многолетних исследований команда специалистов Сеченовского университета сфокусировалась на изучении влияния повышенной экспрессии HSPA1A — одного из ключевых представителей семейства белков HSP70 — на развитие нейродегенеративных процессов у трансгенных мышей. В одном из последних экспериментов использовалась модель FUS-ассоциированной нейродегенеративной патологии, которая близка по своим проявлениям к определенной форме БАС у человека.
«Мы наблюдали, что усиленная экспрессия HSP70 помогает клеткам гораздо лучше справляться с накоплением патологических белков, эффективно предотвращая их агрегацию и защищая нейроны от преждевременной гибели»,
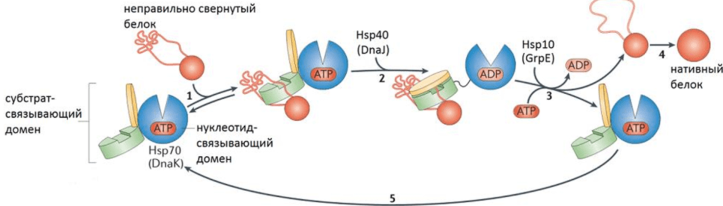
Белки HSP70 широко известны своей незаменимой ролью в поддержании протеостаза — деликатного баланса между синтезом, правильным сворачиванием и контролируемой деградацией белковых молекул в клетке. В условиях стресса или при развитии заболевания эти белки выступают в роли «спасателей», помогая восстанавливать поврежденные белки и предотвращая их токсическое накопление, которое может привести к клеточному повреждению.
Экспериментальные данные показали, что у мышей с моделью FUS-ассоциированного нейродегенеративного процесса наблюдалось заметное снижение уровня нейродегенерации в различных отделах мозга. Примечательно, что защитный эффект HSP70 распространялся не только на спинной мозг и кору головного мозга, но и на лимбическую систему — область, тесно связанную с регуляцией эмоций и поведения. Этот аспект исследования крайне важен, поскольку он открывает перспективы для сохранения когнитивных и эмоциональных функций, которые часто значительно страдают при развитии нейродегенеративных состояний.
Кроме того, исследователи успешно установили безопасность введения рекомбинантного HSP70 для лабораторных мышей. В проведенных экспериментах не было выявлено никаких заметных структурных изменений в тканях мозга, печени, селезенки или тимуса даже при достаточно высоких дозах HSP70, достигающих 500 мкг/кг. Эти данные дают веские основания полагать, что белок может быть безопасен для системного применения в будущем. Важным открытием стало также то, что защитное действие HSP70 зависит от его внутриклеточной или внеклеточной локализации: внутриклеточный белок эффективно замедляет дегенерацию, в то время как внеклеточный вариант, напротив, может способствовать усилению повреждения нейронов. В рамках этой масштабной работы были также разработаны и применены передовые методы анализа, включая количественное иммунофлуоресцентное картирование и раман-спектроскопию с использованием алгоритмов машинного обучения.
Ученые подчеркивают, что полученные результаты однозначно указывают на высокий терапевтический потенциал белка HSP70 в лечении нейродегенеративных заболеваний. И хотя на данном этапе речь идет о доклинических моделях, эти открытия закладывают прочную основу для дальнейших исследований и разработки нового поколения препаратов, способных активировать естественные защитные функции этих важнейших белков в организме человека.