Искусственный интеллект создает детальную цифровую модель фиброза сердечной ткани
Специалисты из МФТИ разработали нейросеть, способную формировать высокоточную цифровую карту здоровых и поврежденных фиброзом клеток сердечной ткани на основе микроскопических данных. Эта инновационная компьютерная модель позволила ученым глубже изучить механизмы развития аритмии при фиброзе, а также оценить воздействие препарата верапамил на эти процессы. Ожидается, что данная технология значительно повысит эффективность хирургического вмешательства, обеспечивая более точную диагностику и оптимизацию планов лечения.

Михаил Словицкий, старший научный сотрудник лаборатории экспериментальной и клеточной медицины Института биофизики будущего МФТИ, акцентирует: «Это не просто эффектное изображение; в будущем каждый подобный `цифровой двойник` сердца способен предотвратить повторные операции и осложнения у десятков пациентов с фиброзом, спасая их жизни».
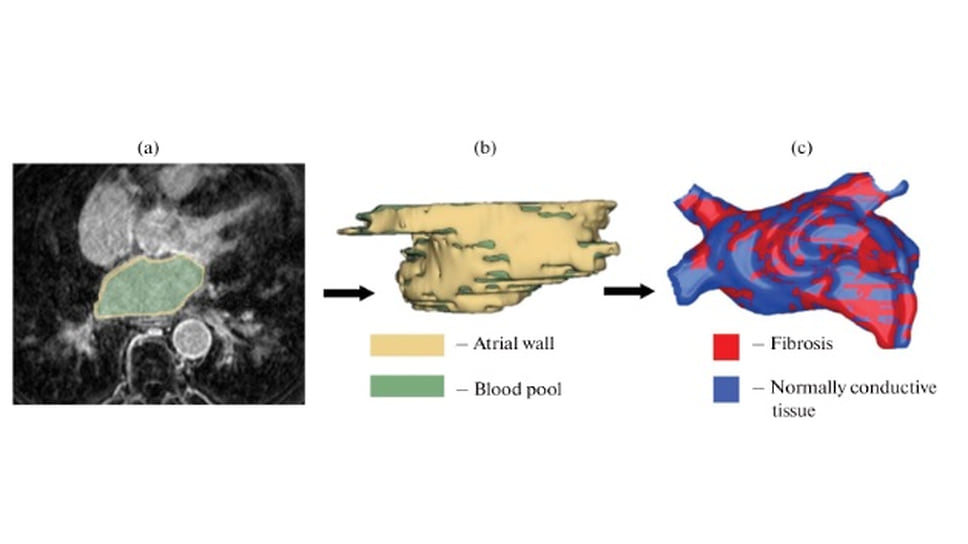
Для создания этих детализированных изображений исследователи проанализировали сотни снимков сердечных тканей, полученных с помощью конфокального микроскопа, а также аннотированные гистологические данные пациентов с фибрилляцией предсердий, предоставленные ГКБ №23 им. И. В. Давыдовского и ГБУЗ МО МОНИКИ им. М. Ф. Владимирского. На основе этой информации был разработан алгоритм, способный выявлять мельчайшие клеточные изменения и с высокой точностью реконструировать расположение фиброзных волокон для каждого конкретного пациента.
Валерия Цвелая, руководитель лаборатории экспериментальной и клеточной медицины Института биофизики будущего МФТИ, пояснила: «На изображении розовым цветом обозначены здоровые кардиомиоциты – клетки соединительной ткани, ответственные за передачу электрических импульсов. Желтым показаны коллагеновые волокна, а синим – фибробласты, то есть клетки, пораженные фиброзом, в которых нарушается проведение импульсов. На данный момент это лишь пилотный образец, полученный с помощью микроскопии. В наших ближайших планах – научить искусственный интеллект создавать аналогичные карты на основе данных КТ, а затем и МРТ. Это позволит визуализировать болезнь с гистологической точностью, но при этом абсолютно безболезненно и без инвазивных процедур».

Хирурги смогут применять эту «виртуальную копию» предсердной ткани не только для планирования операций, но и в качестве своего рода «виртуального полигона» для тестирования эффективности различных медикаментов.
Фибрилляция предсердий – состояние, при котором избыточное разрастание рубцовой ткани нарушает электрическую проводимость сердца и вызывает аритмию – затрагивает миллионы людей по всему миру. Основная трудность заключается в уникальности паттерна фиброза у каждого пациента. Для выбора оптимальной стратегии лечения врачам критически важно понимать особенности патологии на клеточном уровне.
Разрабатываемая учеными МФТИ компьютерная модель призвана решить эту сложную задачу. В недавнем исследовании она уже доказала свою эффективность, позволив детально проанализировать распространение электрических импульсов в сердце, пораженном фиброзом, а также изучить влияние препарата верапамил на эти процессы.
Интересно, что сам по себе фиброз не всегда является прямой причиной нарушений сердечного ритма. При сохранении нормальных электрических свойств сердечных клеток фиброзные участки не провоцируют устойчивую аритмию. Истинная опасность возникает при продолжительной фибрилляции: когда электрофизиология клеток претерпевает изменения, фиброзные ткани начинают функционировать как «мостики» для беспорядочных электрических импульсов.
Особо значимым стало выявление двойственного действия верапамила. В случаях, когда электрофизиология сердца оставалась в норме, препарат, напротив, увеличивал вероятность аритмии при наличии фиброза. Однако у пациентов с хронической фибрилляцией предсердий верапамил демонстрировал противоположный эффект, нормализуя проведение импульсов и эффективно подавляя опасные циркулирующие волны возбуждения. Этот факт подчеркивает критическую важность персонализированного подхода: эффективность препаратов зависит от конкретной клинической картины, что требует глубокого понимания состояния болезни каждого пациента.
Эта передовая технология представляет собой важный шаг к внедрению персонализированной кардиологии. В будущем она позволит хирургам максимально точно планировать операции, учитывая индивидуальные особенности сердечной ткани каждого пациента, а также подбирать оптимальную фармакотерапию, основываясь на прогнозируемом моделью эффекте различных лекарственных средств.