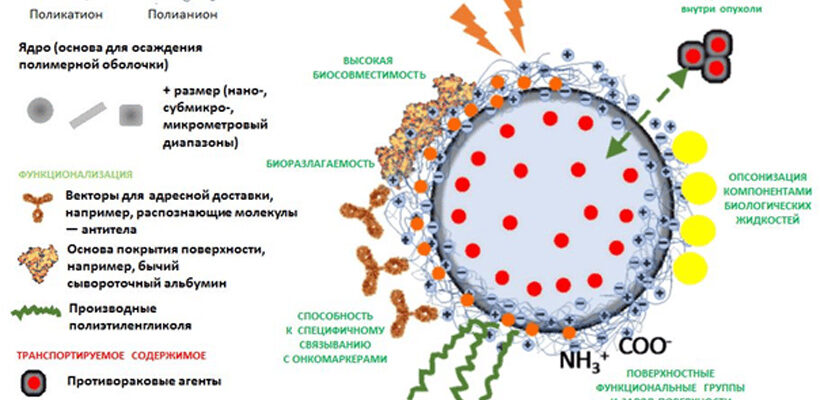
Эффективность любого лекарства напрямую зависит от его способности точно достигать пораженных болезнью клеток, минуя при этом здоровые органы. Этот принцип лежит в основе современных исследований в области прецизионной доставки медикаментов, где нанотехнологии играют ключевую роль.
- Интервью с профессором Сколтеха Глебом Сухоруковым
- Почему адресная доставка лекарств так важна?
- История и развитие систем доставки
- Размеры и типы систем доставки
- Медицина будущего на клеточном уровне
- Основные подходы к точечной доставке сегодня
- Методы активации систем доставки
- Области применения адресной доставки наночастиц
- Новые возможности для лечения мозга
- Управление и навигация наночастицами
- Доставка, зависящая от кислотности среды (pH-чувствительные системы)
- Безопасность наночастиц
- Биополимерные покрытия для имплантатов: путь к практике
- Перспективы наночастиц
Интервью с профессором Сколтеха Глебом Сухоруковым
Почему адресная доставка лекарств так важна?
Профессор Глеб Сухоруков подчеркивает, что развитие систем адресной доставки лекарств имеет такое же, если не большее, значение, как и открытие самих действующих веществ. Классическая химиотерапия, например, неизбирательно поражает как опухоль, так и здоровые ткани, вызывая массу побочных эффектов. Целенаправленная доставка медикаментов к очагу заболевания позволяет значительно повысить эффективность лечения и одновременно минимизировать вред для здорового организма. К тому же, многие новые лекарственные соединения плохо растворимы в воде, что требует их инкапсуляции в микро- или наноформы для эффективной транспортировки в кровотоке и точной доставки.
История и развитие систем доставки
Поиск эффективных способов доставки лекарств исторически развивался на стыке коллоидной химии и физики. Среди первых успешных систем были липосомы — сферические контейнеры, состоящие из натуральных липидов, которые легко сливаются с клеточными мембранами. Позже стали активно применяться частицы из биоразлагаемых полимеров, таких как полимолочная кислота, обладающие предсказуемыми свойствами распада в организме.
Размеры и типы систем доставки
Для эффективной циркуляции в кровотоке частицы должны быть крайне малы, обычно до 1 микрона. Однако возможно использование и более крупных носителей, например, собственных клеток крови пациента. Отдельным, активно развивающимся направлением являются тонкие, микронные по толщине покрытия на поверхности имплантатов, которые также служат системами адресной доставки.
Медицина будущего на клеточном уровне
Глеб Сухоруков видит будущее медицины в способности взаимодействовать с отдельными живыми клетками. Он проводит параллель с беспилотными системами, которые могут мониторить каждый квадратный метр поверхности земли, и предполагает, что в будущем наука достигнет возможности мониторинга и точечного воздействия на клетки организма с высоким разрешением. Это позволит на ранних этапах диагностировать и прецизионно устранять любые патологии.
Основные подходы к точечной доставке сегодня
В настоящее время используются два ключевых метода:
- Целевое накопление: Система доставки разрабатывается таким образом, чтобы она избирательно взаимодействовала с определенной тканью (например, костной при установке имплантата), накапливалась в ней и оказывала терапевтический эффект самостоятельно или под внешним воздействием.
- Внешняя активация: Частицы циркулируют по всему организму, но активируются только в пораженных тканях с помощью внешнего стимула. Неактивированные частицы безопасно выводятся из организма, не нанося вреда.
Методы активации систем доставки
Для «открытия» контейнеров с лекарством или «наведения удара» по искусственным мишеням применяются различные внешние воздействия:
- Ультразвук: Часто используется для высвобождения лекарств из наноконтейнеров.
- Магнитные частицы: Доставляются к патологическим клеткам, а затем с помощью переменного магнитного поля вызывают локальный нагрев, уничтожая пораженную ткань.
- Бор-нейтронозахватная терапия: Бор доставляется к аномальным клеткам. При облучении нейтронами он испускает альфа-частицы, которые локально уничтожают соседние клетки в радиусе нескольких микрон.
- Световое воздействие: Хотя возможно, но менее практично для глубоких тканей, так как требует ввода инвазивного волновода.
Области применения адресной доставки наночастиц
- Опухоли: Являются наиболее изученной и относительно доступной целью для адресной доставки. Наночастицы изначально разрабатывались для онкологии, и в этой области достигнуты значительные успехи. Важно отметить, что даже если основная часть введенных частиц оседает в печени, их активация происходит только в области опухоли.
- Сердце и почки: Доставка может осуществляться через катетер, введенный в артерию, ведущую к конкретному органу, с подбором размера частиц для их удержания.
- Мозг: Преодоление гематоэнцефалического барьера остается серьёзным вызовом. Однако временное открытие барьера с помощью ультразвука уже используется в клинической практике.
Новые возможности для лечения мозга
В мозг могут доставляться не только лекарства, но и специальные частицы, такие как магнитоэлектрические или пьезочастицы. Эти частицы сами по себе не являются лекарством, но позволяют электрически стимулировать нейроны извне с помощью переменного магнитного поля или ультразвука. Это открывает значительные перспективы для лечения эпилепсии, деменции, болезней Альцгеймера и Паркинсона, предлагая замену громоздким имплантируемым электродам на микроскопические частицы.
Управление и навигация наночастицами
Направлять носители магнитным полем пока остается сложной задачей; оно эффективно лишь для удержания частиц в уже достигнутом органе. Идея оснащения крошечных частиц «моторами» для самостоятельного движения остается в области научной фантастики из-за их крайне малого размера. Однако концепция нанороботов, способных диагностировать и ремонтировать на клеточном уровне, очень привлекательна. Более крупные «умные пилюли» (миллиметрового размера), предназначенные для желудочно-кишечного тракта, уже могут управляться магнитами.
Доставка, зависящая от кислотности среды (pH-чувствительные системы)
Системы доставки могут быть спроектированы так, чтобы избирательно реагировать на уровень pH. Например, контейнеры, устойчивые в кислой среде желудка, но разрушающиеся в слабощелочной среде кишечника. Учитывая, что опухоли часто имеют слегка пониженную кислотность, можно создавать системы, высвобождающие лекарство именно там.
Безопасность наночастиц
Вопреки ранним опасениям, термин «нано» относится исключительно к размеру, а не к химическому составу. Токсичность определяется веществом, а не его масштабом. В медицинских целях используются строго разрешенные и биоразлагаемые полимеры (как полимолочная кислота), которые распадаются на нетоксичные компоненты и вводятся в минимальных, микрограммовых количествах, что делает их безопасными для организма.
Биополимерные покрытия для имплантатов: путь к практике
В настоящее время более быстрый и успешный путь к клиническому применению имеют биополимерные покрытия для имплантатов. Эти разработки уже активно помогают пациентам благодаря относительно низким регуляторным барьерам.
Любая имплантация сопряжена с рисками инфекции и воспаления. Покрытия позволяют наносить антибиотики и противовоспалительные вещества непосредственно на поверхность медицинских изделий (иглы, катетеры, стенты, протезы). Это обеспечивает локальное воздействие, значительно снижая дозу препарата по сравнению с системным введением.
Активное вещество встраивается в тонкую полимерную пленку (из полимолочной кислоты или других биополимеров), которая «ламинирует» поверхность изделия. По мере расщепления полимера лекарство постепенно высвобождается. Длительность высвобождения может быть точно настроена: от нескольких минут (с ультразвуковой стимуляцией) для урологических процедур до нескольких месяцев (например, 4-6 месяцев для желчевыводящих стентов), в зависимости от медицинских требований. Для объектов сложной формы используются технологии 3D-биопечати, позволяющие наносить покрытие с высокой точностью.
Команда профессора Сухорукова активно работает над желчевыводящими стентами (с ГКБ №31), урологическими катетерами (с МНОЦ МГУ), антибактериальными покрытиями для костных имплантатов, включая 3D-печатные протезы тазобедренного сустава (с СамГМУ), а также костными наполнителями (с СибГМУ), которые пока находятся на стадии доклинических испытаний.
Перспективы наночастиц
Несмотря на текущий акцент на покрытиях, наночастицы, безусловно, придут в широкую клиническую практику. В некоторых странах они уже используются для дорогостоящего лечения. Продолжаются активные исследования, в частности, в области стимуляции клеток мозга и лечения нейродегенеративных заболеваний, обещая новые прорывы в будущем.